文|未來醫編輯室
諮詢專家|亞東紀念醫院泌尿外科主任鍾旭東醫師
攝護腺癌的盛行率與風險因子
攝護腺癌是全球男性中第二常見的癌症,特別好發於年長男性,超過一半的病例發生在70歲以上。根據最新癌症登記報告,台灣111年新發生攝腺癌高達9,062人,位居癌症增加比例第一名[1]。攝護腺癌年齡範圍涵蓋40歲到90歲以上,也有少部份屬於45歲以下的個案,而通常越早發通常預後較不理想。除了年齡之外,攝護腺癌風險統計上顯示出人種差異,非洲裔男性的罹病風險高於白人,而亞洲男性的發生率相對較低。
遺傳因素也會影響攝護腺癌風險,研究認為有家族史的男性,特別是父親罹患轉移性或高風險攝護腺癌者,或三等親以內有三位以上男性曾罹病者,皆屬於高遺傳風險族群。特定基因突變也與攝護腺癌有關,目前最明確的是帶有BRCA1、BRCA2基因突變的男性,攝護腺癌風險可能高達3.8-8.6倍[2],遺傳性癌症基因突變往往也與較早發病年齡及更高轉移機率有關係。其他參與DNA修復的基因如MLH1與MLH2若出現異常,也可能增加罹癌風險。
特定生理特徵以及荷爾蒙濃度,也被認為與攝護腺癌有關。研究指出身高較高的男性與體重過重者,罹患攝護腺癌機率略為增加,這可能與IGF-1或代謝症候群有關。內分泌系統中的類胰島素生長因子(IGF-1)濃度過高與攝護腺癌風險上升之間相關聯,可能會促進細胞生長與癌變,部份研究認為,服用降血糖藥物與較低的攝護腺癌有關[3]。
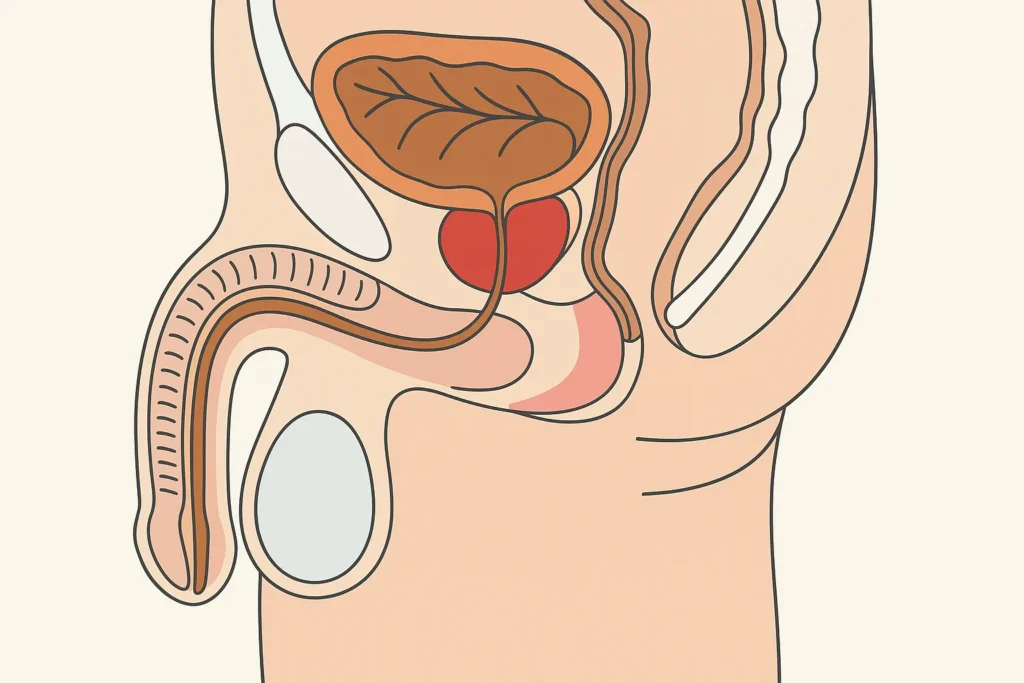
攝護腺癌的症狀與診斷
攝護腺癌是男性常見的癌症之一,但由於其發展過程緩慢、早期症狀不明顯,許多患者在癌症初期並不自知。雖然目前不建議對所有男性進行常規攝護腺特異抗原(PSA)檢測,以避免過度診斷與治療,但特定高風險族群仍可與泌尿科醫師討論後,進行定期監測與早期檢測。
PSA是一種由攝護腺細胞分泌的蛋白質,其在血液中的濃度升高可能是攝護腺癌的警訊。不過,由於良性攝護腺增生(BPH)也可能造成PSA升高,因此單一數值並無法斷定是否為惡性病變。目前認為,年齡超過50歲的男性,或是有攝護腺癌家族史、非裔族群45歲以上男性,以及具有BRCA1或BRCA2基因突變、年齡超過40歲的男性,普遍認為應提高警覺,與專科醫師共同評估是否進行PSA檢測。
臨床觀察發現,早期攝護腺癌往往沒有明顯症狀。許多個案是在腫瘤生長到足以壓迫膀胱或尿道時,才會開始出現泌尿異常如排尿頻率增加、急尿、夜尿、尿流變細或排尿困難等,但這些症狀與良性攝護腺肥大高度重疊,使得初期辨識更加困難。當癌症進一步惡化,尤其是轉移到骨頭時,患者可能會感到腰背或骨盆的持續性疼痛。
值得注意的是,攝護腺癌的骨轉移有時會被誤認為單純的骨刺或關節問題,直到疼痛惡化或伴隨神經壓迫症狀如下肢無力、大小便失禁時,才經進一步影像檢查確診為晚期攝護腺癌。
此外,若發現尿液或精液帶血、勃起功能障礙等問題,也應及時就醫檢查。這些變化雖然不一定直接來自癌症,但也可能是早期警訊。尤其對於本身就屬於高風險族群的男性應提高相關症狀的警覺。

攝護腺癌的分級與預後
攝護腺癌分期目前多採用TNM系統進行分類,T代表原發腫瘤的大小與範圍,N則評估是否有鄰近淋巴結轉移,M則判定癌細胞是否已轉移至遠端器官。攝護腺癌可分為四個主要期別,並結合PSA指數與格里森分數,進一步評估復發風險。
■第一期:癌細胞侷限於攝護腺內的一小部分,通常無法在肛門指診中觸及,也沒有淋巴或遠端轉移,屬於早期局限型,常因PSA異常升高而經由切片診斷發現。這類癌症多屬於極低度或低度復發風險。
■第二期:癌症雖仍在攝護腺內,但已擴大至單葉的一半以上,甚至可能侵犯到雙葉。此期仍無淋巴結或遠端轉移,但復發風險相對提升,部分患者可能屬於中度復發風險族群。
■第三期:癌細胞突破攝護腺外膜甚至擴散至儲精囊,即所謂的「局部晚期」攝護腺癌。雖然尚未發現明顯的淋巴或遠端轉移,但腫瘤已脫離原位,威脅周邊組織,需更積極介入治療。
■第四期:癌症進一步擴散到鄰近器官如直腸、膀胱,或轉移至淋巴與遠端部位,便屬於第四期轉移性攝護腺癌。根據統計,有高達三分之一患者在確診時已出現遠端轉移,常見轉移部位包括骨頭、淋巴結、肺臟與肝臟,代表病情已進入難以手術根治的階段。
除了TNM分期,醫師還會綜合患者的PSA值與病理切片格里森分數進行風險分類。侷限型攝護腺癌可根據PSA濃度(如低於10、10至20或高於20 ng/ml)、臨床分期(T1至T3a)以及格里森分數(從6到10)進一步區分為極低度、低度、中度與高度復發風險。若腫瘤已侵犯出攝護腺或合併轉移,則多屬於極高度復發風險群,須進行更全面的系統性治療。
「格里森分數」(Gleason score)是臨床上用來評估攝護腺癌惡性度最重要的指標之一。根據細胞與正常攝護腺細胞的相似程度,將其分為1分到5分。1分與2分已不再常用於現代病理報告中,臨床上格里森分數通常從3分起才視為癌細胞,其中5分惡性程度最高。舉例來說,若在顯微鏡下病理科醫生發現癌細胞占比最高的分數是3分,次高比例的是4分,則格里森分數為3+4=7分。格里森分數5級(即總分9分和10分:4+5, 5+4, 5+5)是惡性度、復發率最高的一級。攝護腺癌一旦發生骨轉移將明顯影響預後與存活,統計顯示,將近80%的晚期攝護腺癌會發生骨轉移[4],特別是分化不佳、格里森分數較高者,骨轉移比例更高。
■等級1:格里森分數為6分或更低。細胞分化良好,與正常攝護腺組織相似,侵襲性較小,生長緩慢,不太可能擴散。
■等級2:格里森分數為3+4=7分。屬於中度侵襲性,生長和擴散的可能性中等。
■等級3:格里森分數為4+3=7分。腫瘤生長及擴散速度較3+4=7分者更快。
■等級4:格里森分數為4+4=8分。屬於較高惡性度,腫瘤生長和擴散速度快。
■等級5:格里森分數為9或10分 (如5+4, 4+5, 5+5)。分為最惡性的攝護腺癌,腫瘤生長速度相當快,9-10分者的生長速度甚至是8分者的2倍。格里森分數10分表示癌細胞分化不良且高度侵襲性。
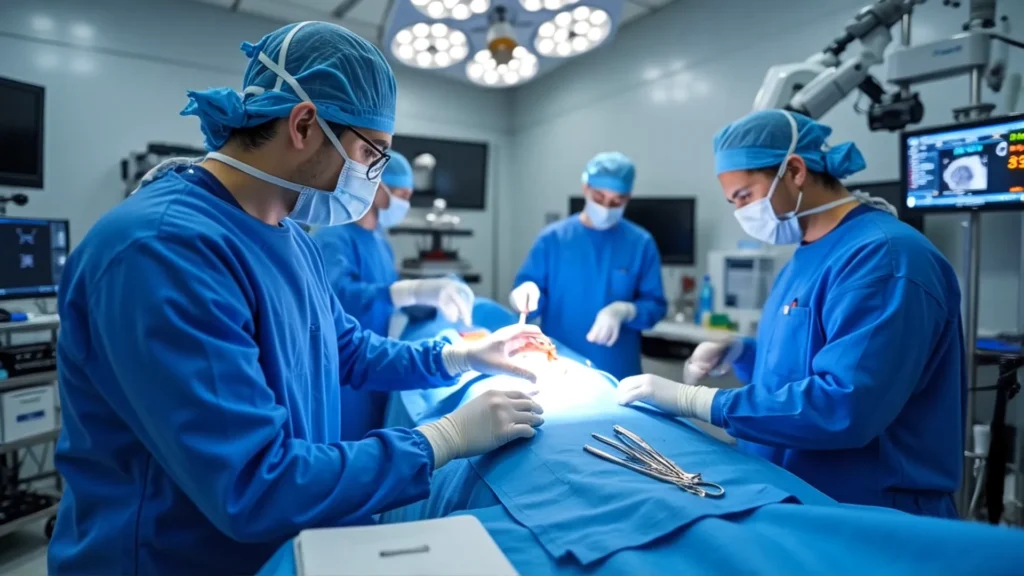
攝護腺癌的治療與選擇
攝護腺癌的治療策略相當個人化,從最保守的觀察等待到尖端的標靶治療與最新的放射治療,會依據癌症分期、風險程度、病患年齡、身體狀況進行治療安排。對於侷限性攝護腺癌,多以治癒為目標,主要方法包含手術、放療或積極監控。如果屬於已經轉移的晚期癌症,則著重於延長生命、減輕症狀及維持生活品質。
對於極低度或低度復發風險的患者,特別是年長或罹患其他重症的病人,臨床上多採取積極監控或觀察性等待策略。積極監控強調定期檢查,包括PSA抽血、肛門指診與攝護腺切片,追蹤是否有病情惡化跡象,如PSA異常上升或病理分數惡化,才考慮進一步治療。若病患年紀更高或罹患其他高死亡率疾病,則可能選擇觀察性等待,在無症狀時不積極治療,待有骨痛等症狀出現時再進行緩解性治療。
手術方面,攝護腺根除術是侷限性癌症的主要治療方式。近年達文西機械手臂進行的攝護腺癌微創手術已相當普及,手術傷口小、出血量少與恢復快等優勢。與傳統開腹或腹腔鏡手術相比,達文西手術在出血控制與術後疼痛方面效果更佳,且住院天數較短。不過,即使是微創手術,仍有可能引發尿失禁或勃起功能障礙,特別是在神經無法保留的情況下,約有小比例患者可能需長期尿布使用,勃起功能恢復則取決於神經保留程度。
另一常見治療方式是放射線治療,適用無法手術或拒絕手術的患者。放療分為體外放射與近接放療(體內放射線治療),後者可將放射源直接植入攝護腺內,以減少對周圍器官的輻射影響,但仍有一定機率出現排尿困難、膀胱或直腸刺激,以及勃起障礙等副作用,亦有部份在治療1至2年後才逐漸顯現,尤其為直腸刺激症狀。
攝護腺癌放射性治療能結合標靶與放療的特性。鐳-223專門針對骨轉移,透過短距離放射殺死癌細胞,副作用相對輕微;鎦-177 PSMA治療則鎖定表現PSMA的癌細胞,以更高精準度進行破壞,被證實在轉移性去勢抗性攝護腺癌病人中有效。
一般而言,進入轉移性的攝護腺癌通常會需要全身性治療,包括荷爾蒙治療、化學治療、標靶藥物、免疫治療,以及雄性素抑制劑與PARP抑制劑(適用BRCA或其他HRR基因突變者)等新興治療。
■荷爾蒙治療:攝護腺癌生長仰賴睪固酮,荷爾蒙治療的目的就是降低體內睪固酮濃度。可透過注射藥物或進行睪丸切除手術達成。對轉移性攝護腺癌或術後復發風險高的病人效果顯著,雖無法根治,但能顯著延緩病情惡化。副作用包括性功能減退、骨質疏鬆、體重增加及心血管風險等副作用。當荷爾蒙治療無效則可能進展為所謂「去勢抗性攝護腺癌」(CRPC),需改用其他治療方式應對。
■化學治療:治療轉移性攝護腺癌的重要策略,特別適用於剛診斷轉移病灶時,與荷爾蒙治療同步使用可明顯延長存活期。使用docetaxel等藥物治療可延壽一年以上,即便在病人荷爾蒙治療失效、進展為CRPC時,也仍可透過化療緩解症狀與延長壽命。雖然化療可能帶來噁心、掉髮與白血球下降等副作用,但多數病人可順利完成療程,副作用亦可控制。
■標靶治療:在晚期攝護腺癌治療中逐漸重要,以PARP抑制劑Olaparib最具代表性,適用帶有BRCA1/ 2或其他HRR突變的CRPC病人。此藥物能阻斷癌細胞DNA修復機制,進一步促使癌細胞死亡。研究證實能顯著延長病人平均存活期,健保也於2023年底有條件納入給付範圍。
攝護腺癌的預防與檢查建議
現代男性壽命延長,攝護腺癌發生比例並不低,目前大多建議50歲以上的男性定期接受攝護腺檢查,具有遺傳風險的族群,例如父親或兄弟罹病者,或帶有BRCA基因突變的男性,應及早與醫師討論是否提前進行PSA篩檢與攝護腺評估,有助於早期發現病變。
目前攝護腺檢查工具包括攝護腺超音波、觸診和PSA抽血檢查(癌症指數偏高者更要注意),過去若評估高機率為惡性攝護腺癌,臨床上會採取經扛門的探針切片,但難以避免診斷準確率問題。現在則有結合核磁共振與超音波的穿刺切片,透過影像導航得到更精準的攝護腺癌診斷,MRI導引切片常採經會陰路徑,相較於經直腸切片感染風險較低還能減少術後感染風險。
管理個人健康尤其是體重控制、健康飲食,是預防癌症的根本。統計顯示,肥胖與攝護腺癌風險上升有關,而均衡攝取富含蔬果、低脂、含鈣與維生素D的食物,有助於整體代謝與骨骼健康。規律運動則可幫助維持體重、改善荷爾蒙代謝,也能減少雄性素剝奪療法造成的副作用,並提升生活品質。
此外,戒菸與限制飲酒亦可降低癌症發生。吸菸對免疫系統與細胞修復造成不良影響,過量飲酒則可能擾亂荷爾蒙平衡。總之,預防攝護腺癌應從定期健康檢查與及時就醫著手,特別是高齡男性出現排尿困難、頻尿或不明骨痛等症狀時,應及時接受泌尿科評估,避免延誤攝護腺癌的早期診斷。

[1] 111年癌症登記報告,https://www.hpa.gov.tw/Pages/List.aspx?nodeid=269
[2] BRCA2 gene mutation and prostate cancer risk,https://pmc.ncbi.nlm.nih.gov/articles/PMC7001059/
[3] Metformin therapy and risk of cancer in patients with type 2 diabetes: systematic review,https://pubmed.ncbi.nlm.nih.gov/23936520/
[4] Prostate cancer bone metastases biology and clinical management (Review) ,https://pmc.ncbi.nlm.nih.gov/articles/PMC10028493/